|
Свой на Aqa.ru
     |
о проводимости...... (страница 2) |
|
электропроводность водички как я понял зависит не только от общей жесткости и температуры воды, но и от кислотности - чем больше в воде СО2 и соответственно угольной кислоты - тем выше проводимость. |
|
|
22/02/2005 23:16:32
#173003 |
|
Посетитель
  |
|
|
Жень, если не сложно, сделай несколько измерений. Чистая вода, немного кислоты, больше кислоты...Вобщем как бы статистику собрать когда проводимость начнет реально меняться. И Ph отследить. У тебя вроде Ph Мерялка есть точная, так что думаю будет интересно. |
|
|
02/03/2005 10:20:28
#175433 |
|
|
|
Завсегдатай
    |
Практика-критерий истины (страница 2) |
|
Два года назад на форуме поднималась эта тема Проводимость воды |
|
|
02/03/2005 10:25:44
#175436 |
|
Свой на Aqa.ru, Советник
 |
|
|
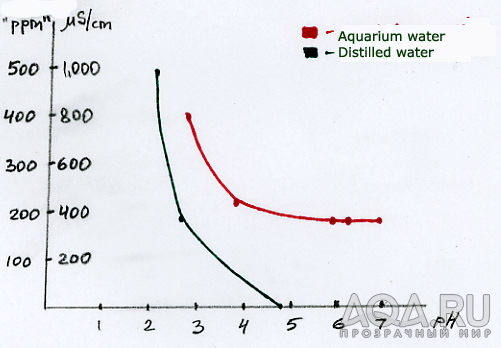
Вот Вам набросок результатов измерений. Измерения проводились электронными измерителями рН и TDS (TDS meter- обычный измеритель проводимости, проградуированный в ррм. Обычно, в этих приборах |
|
|
02/03/2005 10:48:35
#175454 |
|
Посетитель
  |
|
|
Гы. Тенденция понятна. К сожалению график не отражает изменение TDS в "нашем" диапазоне Ph 6-7. Слишком грубо рисовано. |
|
|
02/03/2005 10:51:52
#175458 |
|
Свой на Aqa.ru, Советник
 |
|
|
Дистиллированная вода в "наш" диапазон, увы, не попадает. |
|
|
02/03/2005 10:58:03
#175460 |
|
Посетитель
  |
|
|
Давайте подождем данные других учатстников, любезно согласившихся померять проводимость. Надеюсь их данные будут значительно точнее, того рисунка. |
|
|
02/03/2005 11:08:13
#175465 |
|
Завсегдатай
    |
|
сообщение Michael ....Да... Похоже на нашей воде (КН 13) вряд ли в диапазоне рН 7-8 что-то получиться в результате замеров. Но вот для очень мягкой воды (как у Эдварда) результат наверно будет другой - закономерность будет явно выраженная. ЗЫ. где-то слышал что в воде близкой к дистилату электронные рН метры врут сильно. Вот в этом случае измеритель проводимости может оказаться весьма кстати. |
|
|
02/03/2005 12:43:26
#175520 |
|
Постоянный посетитель, Советник
 |
|
сообщение Fylhtq На мой взгляд, уже проведенные измерения полностью подтверждают те объяснения, которые приводились на протяжении этой ветки. Не думаю, что в данном случае требуются еще какие-либо дополнительные более точные данные. Давайте попробую еще раз повторить то, что уже говорилось здесь раньше: 1) Концентрация ионов кальция в воде средней жесткости - порядка 0.001 моль/литр. 2) Концентрация ионов Н+ в воде с рН=7 равна 0.0000001 моль/литр. 3) Подвижности ионов кальция и Н+ хотя и отличаются, но не так уж существенно, в пределах одного порядка (эти данные вы приводили сами в начале ветки). 4) Из (1,2,3) следует, что для воды средней жесткости с рН=7 вклад ионов Н+ в проводимость будет примерно на 3-4 порядка меньше, чем вклад ионов кальция. 5) Уменьшение рН на единицу повышает концентрацию Н+ на один порядок. Следовательно, в воде средней жесткости вклад ионов Н+ в проводимость может стать сравнимым со вкладом ионов кальция лишь при рН=3-4 (так как при рН=3 концентрация ионов Н+ становится 0.001 моль/литр, что по порядку величины сопоставимо с концентрацией ионов кальция, см. (1) ). 5) Если же взять полностью дистиллированную воду, то в ней ионов кальция и пр. нет, и ее проводимость обеспечивается только ионами Н+ и ОН-. Внесение кислот или щелочей изменяет эти концентрации очень сильно, поэтому в данном случае проводимость и зависит так сильно от величины рН. В идеальном случае, при доливании кислоты или щелочи к полностью дистиллированной воде проводимость должна увеличиваться примерно на порядок при изменении рН на единицу. Вышесказанное можно представить в виде следующих приближенных формул: а) Вклад ионов Н+ в проводимость становится сравнимым со вкладом ионов солей жесткости, если выполняется неравенство: рН (значение GH здесь должно быть выражено в единицах dH, т.е. в немецких градусах). б) Вклад ионов ОН- в проводимость становится сравнимым со вкладом ионов солей жесткости, если выполняется неравенство: рН > 10 + lg(GH) в) Проводимость sigma(pH) дистиллированной воды c добавкой кислоты или щелочи приближенно выражается соотношением: sigma(pH) ~ sigma(7)*ch(2.3*(pH-7)) ~ sigma(7)*10^!pH-7! (Здесь ch - гиперболический косинус, ^ - возведение в степень, !х! - модуль х) Изменено 2-3-2005 автор Dmitrii |
|
|
02/03/2005 14:45:45
#175576 |
|
Посетитель
  |
|
|
Не совсем понятно |
|
|
02/03/2005 15:01:53
#175592 |
|
|
|
Постоянный посетитель, Советник
 |
|
сообщение Fylhtq Не совсем точно сформулировано. Точнее было бы так: При равном изменении рН концентрация ионов H+ изменяется одинаково, как в воде, содержащей ионы кальция, так и без них. Соответственно и абсолютное изменение проводимости должно быть примерно одинаковым в обоих случаях. Другое дело, что для воды, содержащей ионы кальция это изменение будет относительно крайне незначительным, по сравнению с проводимостью, связанной с ионами солей жесткости, а вот для дистиллированной воды - очень значительным, т.к. там этих солей нет. В этом смысле различие между жесткой и дистиллированной водой очень велико. Но абсолютное изменение проводимости - да, должно быть примерно одинаковым в обоих случаях.
А почему вы решили, что это не происходит? Приведенные выше экспериментальные точки вполне согласуются с таким предположением. Посмотрите на значения проводимости дистиллированной воды при ph~3 ph~5, и соответствующие значения для недистиллированной воды - падение проводимости в обоих случаях примерно одинаковое. |
|
|
02/03/2005 15:34:14
#175607 |
|
Посетитель
  |
|
|
Другое дело, что для воды, содержащей ионы кальция это изменение будет относительно крайне незначительным, по сравнению с проводимостью, связанной с ионами солей жесткости, а вот для дистиллированной воды - очень значительным, т.к. там этих солей нет. В этом смысле различие между жесткой и дистиллированной водой очень велико.
Но абсолютное изменение проводимости - да, должно быть примерно одинаковым в обоих случаях. Т.е. фактически при изменении Ph раствора содержащего кальций и не содержащего других примесей (чистой воды)с 7 до 6, проводимость возрастет на 1 -го попугая, образно. Т.е. незначительно. Так? Изменено 2.3.05 автор Fylhtq |
|
|
02/03/2005 15:46:36
#175614 |
|
Постоянный посетитель, Советник
 |
|
|
Ну да, в том смысле, что абсолютное изменение проводимости будет примерно одинаковым - на какие-нибудь x mS/cm, но для жесткой воды это будет лишь незначительная доля общей ее проводимости, а для дистиллированной - весьма заметная ее часть. |
|
|
02/03/2005 16:57:38
#175650 |
|
Посетитель
  |
|
|
Ага. Теперь надо подождать практиков, которые попробуют измерить этого попугая. |
|
|
02/03/2005 16:59:09
#175653 |
|
Постоянный посетитель, Советник
 |
|
|
Если взять подвижность ионов H+ порядка 10^(-2) см2/(B*c), (это, видимо, даже завышенная оценка) то получим, что проводимость воды при изменении pH c pH=7 до pH=6 должна увеличиться всего лишь примерно на 1 микросименс/см. При падении pH до 5 - на 10 микросименс/см, до 4 - на 100 микросименс/см, и т.д. |
|
|
02/03/2005 18:03:52
#175690 |
|
|
|
Постоянный посетитель, Советник
 |
|
|
Результаты домашнего задания: |
|
|
03/03/2005 09:49:12
#175842 |
|
Посетитель
  |
|
|
Спасибо, Евгений |
|
|
03/03/2005 09:59:01
#175845 |
|
Свой на Aqa.ru
     |
|
|
судя по результатам - для реальных банок |
|
|
06/03/2005 23:46:40
#176996 |






 Загружаю
форму....
Загружаю
форму....